2026年2月25日,Nature杂志在线发表了一项来自耶鲁大学陈斯迪(Sidi Chen)研究团队的重磅研究成果显示,通过体内功能筛选策略,鉴定出G蛋白偶联受体家族成员OR7A10作为CAR-NK细胞的“超级增强子”。仅通过单载体过表达OR7A10,即可在不依赖复杂基因编辑的前提下,系统性增强CAR-NK细胞的增殖、活化、代谢适应性及TME抵抗能力,并在多种实体瘤模型中实现完全缓解。
OR7A10属于G蛋白偶联受体(GPCR)家族的嗅觉受体亚家族,传统上认为这类受体仅在嗅觉上皮细胞中表达,负责感知气味分子。此前未有研究报道OR7A10在免疫系统中的功能,这一发现完全突破了领域内的传统认知,为免疫细胞工程化提供了全新的靶点类别。

1、研究背景:寻找CAR-NK细胞的“超级增强子”
面对实体瘤的挑战,科学家们尝试了多种策略,比如给NK细胞装上细胞因子“助推器”,或者敲除其抑制性受体。但这些方法往往工艺复杂或效果有限。来自耶鲁大学陈斯迪教授实验室的团队,独辟蹊径,他们想用一种更简单、更强大的方法:不是做减法(敲除基因),而是做加法(过表达基因)。他们设想,如果能找到一个关键基因,仅仅是在CAR-NK细胞中多表达一份,就能让细胞功能发生质的飞跃,那将极大地简化生产流程,并有可能实现更强的疗效。
2、研究策略:一场大规模的“海选”与精密的“复试”
研究团队设计了一场极其严谨的两步筛选法:
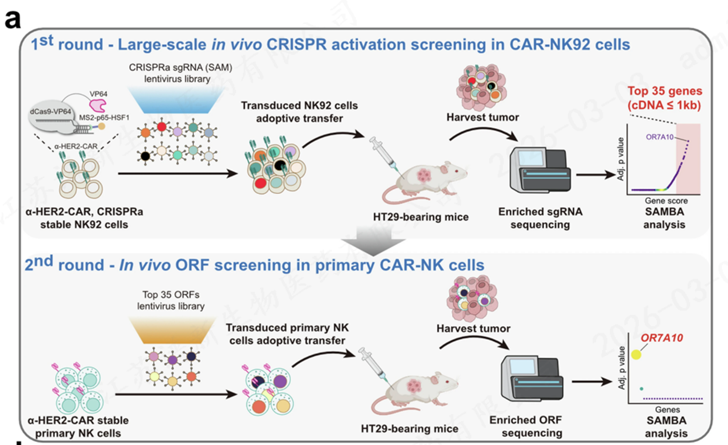
第一轮大规模“海选”(体内CRISPR激活筛选):
他们将一个包含7万多个引导RNA的文库导入CAR-NK细胞中,这个文库可以激活人类基因组中成千上万个基因的表达。然后,将这些经过“地毯式”改造的细胞注射到带有结肠癌的小鼠体内。一段时间后,他们回收那些成功浸润到肿瘤内部的NK细胞,通过高通量测序分析富集的sgRNA,初步筛选出66个可能增强CAR-NK体内抗肿瘤活性的候选基因,其中排名靠前的包括SGSM2、OR7A10、APLN、PDP1和CYB5B等基因。
第二轮精准“复试”(条形码ORF小规模筛选):
为了验证“海选”结果的可靠性,团队构建了一个包含35个顶级候选基因的小型文库,通过专门为分析稀疏数据优化的SAMBA分析方法,对不同时间点、不同肿瘤模型中富集的条形码进行定量分析。他们在真正的人原代CAR-NK细胞中进行验证,再次将其注入小鼠肿瘤模型。结果令人震惊:在所有基因中,OR7A10脱颖而出,成为唯一一个在各个时间点都表现出一致且极显著富集的“冠军”。
3、验证结果:从细胞到动物,从功能到机制的全面碾压
确认OR7A10的潜力后,团队展开了全方位的验证,团队摒弃了复杂的CRISPR基因编辑,直接将OR7A10的cDNA与CAR结构构建在同一个慢病毒载体中,通过一步慢病毒转导,即可同时实现CAR与OR7A10的稳定共表达,无需多步编辑、无需基因敲除。结果令人振奋:
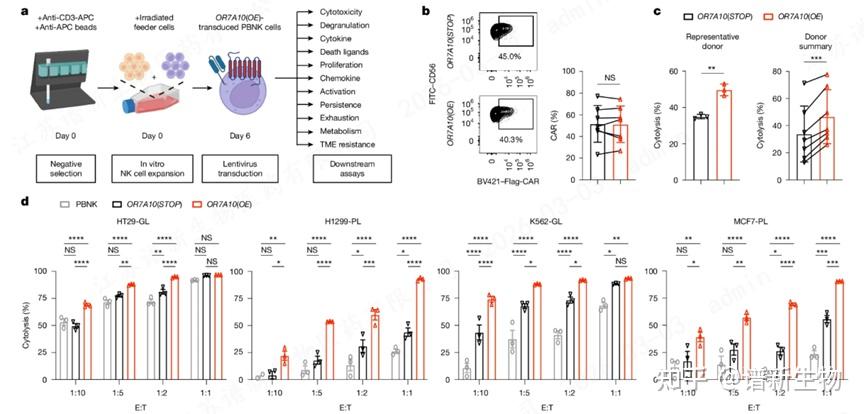
(本文中CAR-PBNK的培养方法为feeder法,可点击此处查阅临床应用)
高效杀伤
来自7位不同健康捐赠者的原代NK细胞,在过表达OR7A10后,对多种癌细胞的杀伤能力显著增强。
于效靶比1:1条件下,其对多种实体瘤细胞的杀伤率较对照组提升40%-70%;
效应分子穿孔素与颗粒酶B的释放量增加2-3倍,死亡配体FasL和TRAIL表达上调1.5-2倍;
促炎细胞因子IFN-γ及TNF-α分泌量提升2-4倍,可有效激活宿主适应性免疫应答;
经反复肿瘤细胞刺激后,OR7A10-CAR-NK细胞表面的耗竭标志物TIM-3、LAG-3及PD-1表达水平较对照组降低20%-40%,展现出更强的抗耗竭能力与持久性。
代谢增强
研究团队发现,OR7A10改造后的CAR-NK细胞线粒体质量显著增强,基础氧消耗率(OCR)提升30%,最大呼吸能力提升45%。这赋予了它们在营养匮乏的肿瘤微环境中生存的能力。
抵抗抑制:在高乳酸、低细胞因子、TGFβ抑制、缺氧等一系列模拟肿瘤恶劣微环境的实验中,OR7A10改造的CAR-NK细胞依然保持了高效的杀伤力,展现出对免疫抑制的强大抵抗性。
信号通路:进一步的机制探索表明,OR7A10作为GPCR家族成员,通过经典的G蛋白信号通路(如cAMP-PKA、ERK、NF-κB)协同并放大了CAR的信号,从而驱动了细胞的全面激活。
完美疗效
在多种实体瘤小鼠模型中,OR7A10改造的CAR-NK细胞都展现了前所未有的疗效:
结肠癌模型:肿瘤生长的近乎完全抑制,治疗后30天肿瘤体积不足100 mm³(对照组约400 mm³),6/6治疗小鼠达到完全缓解,100%长期存活;
原位乳腺癌模型:100%完全缓解 ,所有治疗小鼠(5/5)肿瘤被完全清除,生存时间超过150天,获得长期无瘤生存;而对照组CAR-NK仅能部分抑制肿瘤生长,小鼠平均生存时间不足50天,最终全部因肿瘤进展死亡;
原位卵巢癌腹腔转移模型:所有治疗小鼠都实现了持续的肿瘤控制和长期生存。
治疗过程中,小鼠未出现明显的体重下降或细胞因子风暴迹象。组织病理学分析显示,重要器官未见损伤,且未检测到基因组的致瘤性变异风险。
通过单细胞测序技术,研究人员得以窥见这些“超级细胞”在肿瘤内部的动态变化。数据显示,OR7A10改造的CAR-NK细胞在肿瘤内数量更多,且凋亡相关基因表达下调,存活能力更强。
4、结语与展望
这项研究不仅通过严谨的体内功能筛选找到了一个强大的靶点OR7A10,更重要的是,它开辟了一种全新的CAR-NK细胞工程化策略。与传统复杂的基因编辑不同,只需通过一个载体将OR7A10的cDNA导入细胞,即可显著增强其抗实体瘤能力,这极大地简化了生产流程,使其更具临床转化和“现货型”应用的潜力。
OR7A10就像是为CAR-NK细胞安装的一枚“超级增强子”,不仅强化了其导航、通讯、战斗和续航能力,更赋予了它在极端恶劣环境下生存的韧性。这项研究的成功,为攻克实体瘤带来了新的希望。目前,该技术正在积极推进临床转化,期待它为全球癌症患者带来真正的福音。

苏州市吴中大道1463号越旺智慧谷4号楼