细胞治疗时代来临,为复杂难治性疾病带来希望,CDMO助力其快速发展
2021年,复星凯特的阿基仑赛注射液和药明巨诺的瑞基奥仑赛注射液相继获批,中国迎来两款商业化CAR-T产品。细胞治疗在国内迈入商业化时代,生物技术公司也争相布局细胞治疗产业,细胞治疗究竟为何如此火热,以及CDMO如何助力细胞治疗企业都成为关注热点,本文将从细胞治疗及其CDMO的发展现状和市场趋势等方面进行分析。
细胞治疗采用生物工程的方法获取具有特定功能的细胞并通过体外扩增、特殊培养等处理后,使这些细胞具有增强免疫、杀死病原体和肿瘤细胞等功能,从而达到治疗某种疾病的目的。目前细胞治疗可分为免疫细胞治疗、干细胞治疗及其他体细胞疗法。其中免疫细胞治疗,是指在体外对某些类型的免疫细胞如T细胞、NK细胞、B细胞、DC细胞等进行针对性的处理后再回输人体内,使其表现出杀伤肿瘤细胞,清除病毒等功能。干细胞疗法通常把干细胞培养扩增后回输到患者体内,从而修复组织或进行免疫调节以重建微环境。在临床上较常使用的干细胞种类有间充质干细胞、造血干细胞、脂肪干细胞等。
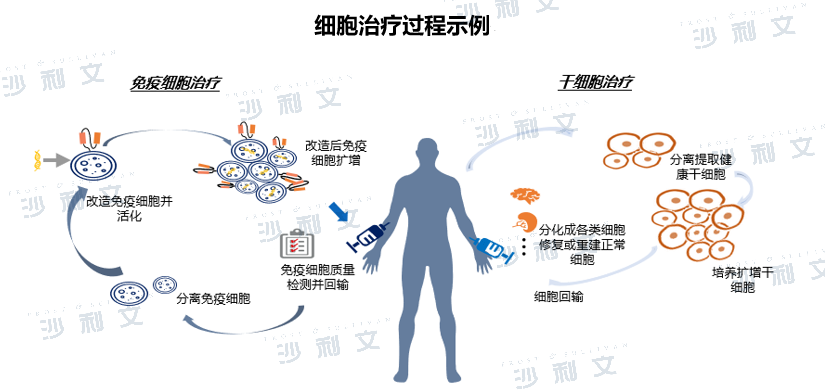
(图片源:Frost & Sullivan)
细胞治疗拥有独特作用机制、相较于传统药物靶向性更强。传统小分子药物不只在病变组织或细胞内分布,还分布于整个机体组织,通常会造成严重的脱靶效应。而细胞治疗优势在于其可主动迁移到靶组织或靶细胞内发挥作用,更大程度上限制药物的毒副作用。
基于独特的作用机制,细胞疗法可为一些传统疗法无效、难治的疾病提供新的治疗选择,并带来长期的疗效。例如,联合化疗方案是目前治疗白血病、淋巴瘤的主要方法之一,尽管可以达到一定的治疗效果,但大部分患者疗效欠佳,存在化疗无效或化疗后复发的情况。而CAR-T在白血病、淋巴瘤、多发性骨髓瘤的治疗中展现出惊艳的治疗效果,通过向T细胞构建人工设计的CAR分子,再将这种改造后的CAR-T细胞回输到患者体内,可特异性赋予病人免疫细胞靶向激活作用,为化疗无效或复发的患者提供新的治疗选择。
对于复杂难治性疾病,细胞治疗相较于小分子和抗体药物临床获益明显。诺华的CAR-T产品Kymriah在治疗复发性或难治性细胞急性淋巴细胞白血病的三期临床试验中表现良好,63名受试者中83%的患者达到了完全缓解,完全缓解的患者均不存在微小残留病灶。
此外,细胞治疗可用以针对特定的病人进行个性化治疗。传统药物的最佳使用剂量因人而异、难以把控。但在细胞治疗中可应用合成生物学设计开关控制药物的合成或释放,根据临床需要设计不同细胞药物以治疗更多疾病。同时,该治疗手段可根据病人的病情发展状态进行动态个性化调整及预后监测。
细胞治疗虽然治疗优势明显,但其研发技术及生产工艺相较于小分子药物和抗体药物存在较多难点。细胞治疗的产业化包括上游的细胞提取和存储、中游的细胞技术研发以及下游的临床应用。其中最大的挑战包括细胞工艺的开发、优化以及生产,细胞产品的工艺流程涉及到细胞的培养、激活、转导、纯化、富集等多个步骤,给规模化生产带来了极大的困难。
细胞治疗产品生产过程的无菌操作、纯度、制备结果的安全性等质量控制对后期的疗效有着重要影响,对于一体化工艺及自动化设备有严格要求。确保生产过程的标准化和稳定性,做到药效和风险可控十分重要。因此,细胞治疗整个研发及生产过程都具有较高的门槛,细胞治疗行业准入壁垒高。
CDMO(Contract Development and Manufacturing Organization),即合同研发与生产组织机构,其职能主要在为跨国药企及生物技术公司提供临床新药工艺开发和制备,以及已上市药物工艺优化和规模化生产服务,包括临床前和临床试验研究用药的生产、以及商业化药品生产。CDMO企业多样化的服务内容和积累的细胞治疗基础研究与开发改造经验可以为细胞治疗企业提供包括细胞库、病毒载体构建、工艺优化、质量检测的服务、临床阶段小规模生产以及后期商业化生产服务。其专业的QA/QC人员和全过程的严格监管,可确保细胞治疗产品的生产符合国家GMP质量标准。

(图片源:Frost & Sullivan)
细胞治疗CDMO可赋能细胞治疗企业,解决其研发与生产的众多难点,帮助降低成本,提高研发效率及商业化成功率。细胞治疗CDMO凭借其研发优势及稳定的生产工艺开辟了独特的细分赛道,成为细胞治疗产业发展的主要推动力之一。
细胞治疗CDMO公司通常拥有大型细胞或载体库,可以帮助药企选择适合的细胞或载体,并进行优化,从而减少试错成本,提高研发效率和成功率。其丰富的生产平台和严格的质检措施也可以帮助药企削减商业化生产成本和时间。此外,一些细胞治疗CDMO公司可以提供一站式新药临床试验申请(IND)和新药上市申请(NDA)等法规相关服务,进一步帮助药企加快研发进度。细胞治疗CDMO可以“多快好省”地完成目标产物的标准化生产,同时也能够满足客户定制化需求,帮助客户完成申报并实现稳定供应。细胞治疗CDMO成为极具潜力的市场领域,极大推动细胞治疗产业的发展。
细胞治疗市场在大量未满足临床需求、新兴技术不断涌现以及利好政策等推动因素下将蓬勃发展,促进细胞治疗CDMO的快速发展
中国肿瘤、神经系统、心血管等疾病的患病人数众多,存在大量尚未被满足的医疗需求。细胞治疗的潜力为肿瘤等各类复杂难治性疾病带来新希望,有望填补目前存在的临床需求。新技术的涌现及临床研究不断深入将拓宽未来细胞治疗市场发展空间,上市的免疫细胞治疗产品目前集中在血液瘤,新型免疫细胞疗法例如TCR-T和TIL将拓展其对于实体瘤的应用。干细胞在神经系统、心血管、自身免疫以及代谢类等疾病领域的研究和临床应用中较为广泛,这类疾病通常治病机理复杂,干细胞可通过组织修复和免疫调节两大功能提供有效治疗选择。目前诱导型多功能干细胞的临床研究逐渐展现出热度,例如Vertex Pharmaceuticals的干细胞衍生疗法VX-880,在对1型糖尿病患者的治疗上表现出优异疗效。
医药研发投入不断增加,刺激创新技术发展,推动市场对新型疗法的需求。2020年,中国医药研发开支约为247亿美元,占全球总开支的12.1%。随着政策、人口、资金红利的推动,预计到2025年,中国医药研发开支将达到496亿美元,占全球医药开支比重的16.8%。同期复合年增长率为15.0%,为全球医药研发开支复合年均增长率的近2倍。研发开支的增长将推动细胞治疗的技术创新与临床转化。
政府不断出台利好政策,促进本土化产品渐露头角。近年内国家不断出台利好政策和指导方针,在明确的指导原则下细胞治疗产业发展逐渐走向规范化。2016年国务院发布的《“十三五”国家科技创新规划》和国家发改委发布的《“十三五”生物产业发展规划》都对细胞治疗领域的产业发展制定了激励政策。政企合作也推动基础研究向高度创新的细胞治疗产业转化,促进细胞治疗产业快速发展。此外,细胞治疗领域资本的关注度不断提升。中国2020年度细胞疗法领域融资总金额约为126亿人民币,2016-2020年复合增长率达到118.8%,融资额逐年攀升。
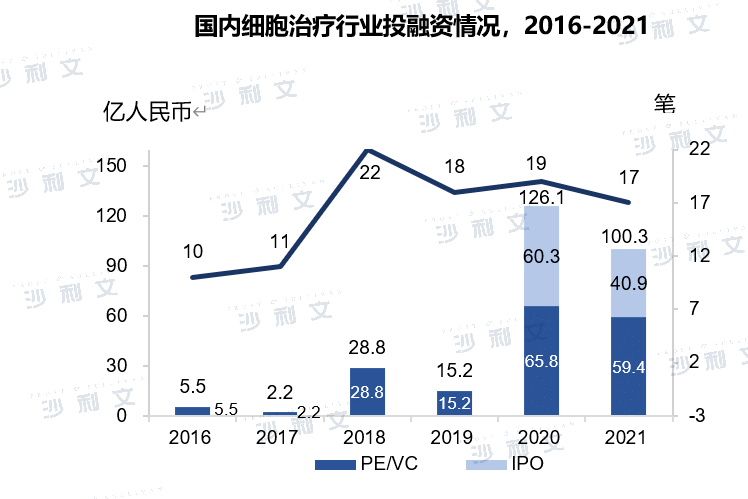
(图片源:Frost & Sullivan)
细胞治疗临床应用潜力巨大,CDMO领域成为未来主流方向之一,与此同时,考虑到细胞治疗的研发和生产特点,对CDMO行业的依赖性,下游企业对于国际化的细胞治疗CDMO需求和粘性将稳定提升,也将催生细胞治疗CDMO的繁荣发展。我国政府对细胞治疗产品的进出口管制严格,同时细胞的特殊属性也使其贮存运输条件更为严格。国内细胞治疗领域短期内供需能力的错配将催生国内细胞疗法相关合同外包产业的蓬勃发展,成为推动CDMO企业发展的刺激点。CDMO市场受终端市场扩容与渗透率提升双轮驱动,发展潜力巨大。
2016年至2020年,全球的细胞治疗CDMO市场规模从5亿美元增至12亿美元,复合年增长率为21.9%。随着细胞治疗相关研究和临床试验的扩大,2020年至2025年的复合年增长率为32.1%,到2030年,全球细胞治疗CDMO市场将达到114亿美元。受中国研发投入高,技术创新及利好政策等的影响,中国的细胞治疗CDMO市场增速将高于全球,2020年至2025年的复合年增长率为46.5%,预计市场规模到2030年将达到38亿美元。
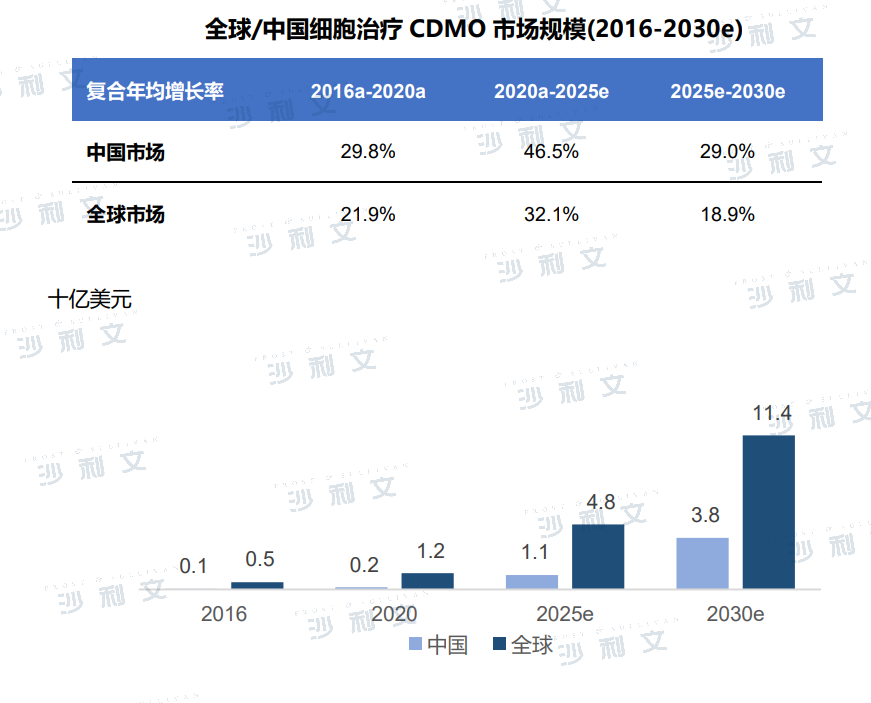
(图片源:Frost & Sullivan)
细胞治疗目前商业化空间大,CDMO极具增长潜力
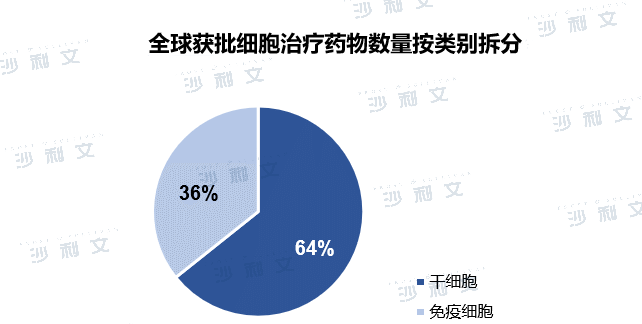
全球细胞治疗市场主要包括干细胞和免疫细胞,获批的细胞治疗产品64%为干细胞治疗,36%为免疫细胞治疗。目前,美国FDA已批准的细胞治疗产品共有19个,其中5款为CAR-T产品。欧洲已批准的细胞治疗产品共有9个,其中3款为CAR-T产品。目前批准的干细胞疗法包括造血干细胞(HSC)、间充质干细胞(MSC),以及在较小程度上的角膜缘干细胞(LSC)。HSC产品主要被批准用于治疗血液疾病,MSC疗法适用于多种疾病,包括心血管疾病、移植物抗宿主病(GvHD)、退行性疾病和炎症性肠病,单个LSC产品被批准用于LSC缺陷。免疫细胞治疗迄今为止获批的治疗产品只有T细胞和DC。T细胞产品是用于血液系统恶性肿瘤的CAR-T疗法,而DC产品则用作实体癌的疫苗。
中国细胞治疗目前只有2款CAR-T产品获批,未有干细胞治疗产品获批。2021年6月,复星凯特的FKC876(阿基仑赛注射液)正式获得NMPA批准,用于治疗复发或难治性大B细胞淋巴瘤,中国迎来首个上市的CAR-T治疗产品。2021年9月,药明巨诺的JWCAR029(瑞基奥仑赛注射液)获批,成为第二款商业化CAR-T产品。中国细胞治疗市场商业化空间大,细胞治疗CDMO极具增长潜力。
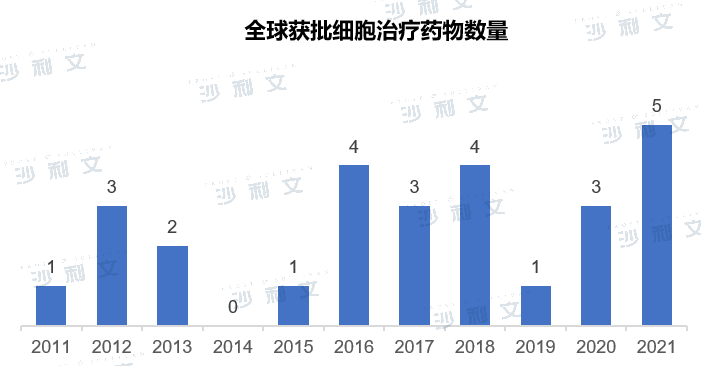
(图片源:Frost & Sullivan)
全球在研的细胞治疗临床试验主要集中在CAR-T和干细胞领域,其他细胞治疗方式仍处于早期研发阶段。根据ClinicalTrials.gov的临床试验来看,近6年全球免疫细胞临床试验数量增长了2倍。以CAR-T为代表的免疫细胞疗法在血液瘤治疗领域不断升级迭代,临床表现优异。目前CAR-T临床研究已开始向实体瘤拓展,未来随着TCR-T,CAR-NK等其他细胞疗法的相继成熟,免疫细胞治疗有望将成为癌症患者的重要治疗途径,进一步提升患者预后。干细胞作为一类具有自我更新和分化潜能的细胞,在神经系统疾病、自身免疫疾病、骨骼和心血管疾病等多领域展现出了极大的潜力。由于其极其广泛的适应症,干细胞相关临床试验数量庞大,在全球正在进行的细胞治疗临床试验中占比超过60%。
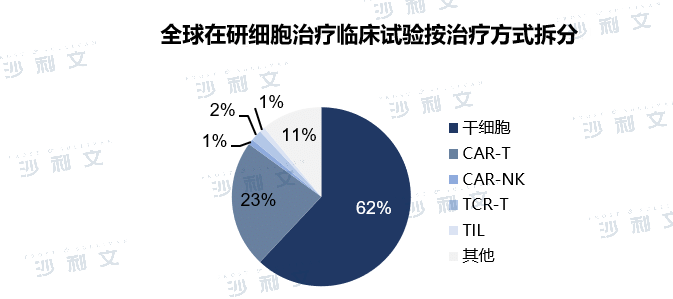
注:临床信息截至2021年10月31日。
(图片源:Frost & Sullivan)
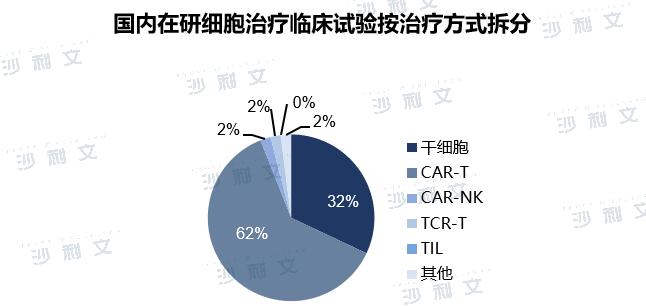
国内在研的细胞治疗临床试验同样主要集中在CAR-T和干细胞领域。中国由于近年来CAR-T产品相继商业化,CAR-T在细胞产品研发中十分火热,占较大比例。根据CDE注册的临床实验来看,中国在研细胞治疗中有约62%为CAR-T相关领域,靶点主要集中在CD19,BCMA等热门血液瘤靶点。目前中国已有两款CAR-T产品获批上市,随着国家鼓励政策的实行以及相关技术的成熟,未来中国将涌现出更多的细胞治疗产品,为肿瘤患者提供有效治疗方式。
中国干细胞治疗发展起步较晚,临床研发目前以间充质干细胞为主,适应症主要包括移植抗宿主病,炎症性肠病,类风湿关节炎,缺血性脑卒中,糖尿病足溃疡等。经过十余年的发展,中国干细胞医疗产业相关技术的日益成熟,监管体系逐步规范化,未来中国干细胞的市场规模也将进一步扩大。从临床阶段来看,中国细胞治疗临床试验中有56%处于临床I期,12%处于临床I/II期,29%处于临床II期,3%处于临床III期。中国细胞治疗临床试验主要处于临床I期阶段,对于细胞疗法的研发仍处于早期。但中国细胞治疗临床试验数量处于全球领先地位,仅次于美国。
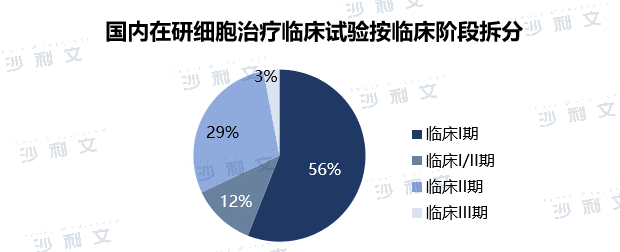
注:临床信息截至2021年10月31日。
(图片源:Frost & Sullivan)
随着更多细胞产品的商业化及渗透率不断上升,全球细胞治疗药物市场规模将从2020年的11亿美元增长至2025年的104亿美元,期间复合年增长率为56.3%,预计于2030年将达到374亿美元。中国细胞治疗产品上市较晚,目前仍处于发展早期,预计2025年、2030年市场规模分别达到88亿以及501亿人民币,期间增速高于全球,2021至2025,2025至2030年的复合年增长率分别为144.6%与41.6%。
细胞治疗产品是近年来全球生物医药市场中增长最快的领域之一,中美两国在免疫细胞疗法临床研发上处于全球主导地位。随着人们对于细胞治疗技术和免疫细胞研究认识的不断深入,全球细胞治疗行业快速发展,大量细胞治疗药物研发进入临床阶段,细胞治疗的安全性和有效性大幅度提升,未来市场前景广阔。中国有望在增长的研发投入和CDMO的推动下弯道超车。
细胞治疗研发与生物工艺壁垒高,CDMO提供结合生物工艺解决方案在内的整体解决方案,可为细胞治疗产业提供全面服务
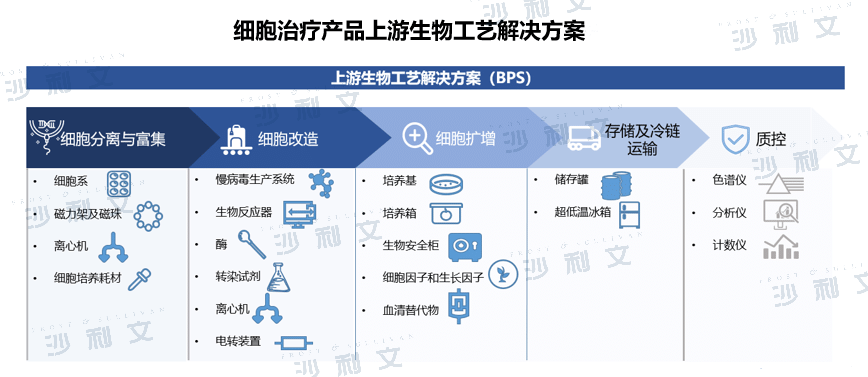
细胞产品相比传统大分子、小分子药物,需要构建细胞库、病毒载体选择及优化,细胞规模化放大培养,对质量检测、批间稳定性、制剂及运输、用药都有严格要求。其中,上游生物工艺解决方案是细胞治疗CDMO行业一大壁垒,包括上游细胞分离、改造及扩增等生物工艺均存在技术难点。由于规模化生产难度大、工艺优化技术壁垒高等研发挑战,企业对于研发生产外包意愿强烈。
提供包括上游生物工艺在内整体解决方案的细胞治疗CDMO能够全面有效地推动细胞产品生产和商业化,具有明显的竞争优势。此外,对于工艺开发与优化、生产成本的控制将成为未来相关企业的核心竞争力。具备药物研究能力、工艺开发能力和生产能力的细胞治疗CDMO,通过全方位的解决方案,从药物研发前端开始渗透,提供定制化服务,帮助企业提高研发效率并控制风险,最终实现细胞产品的商业化。
(图片源:Frost & Sullivan)
国内外重要的细胞治疗CDMO分析
细胞治疗技术快速发展、市场持续扩容,高成本促使海外biotech生产外包意愿强烈,推动CDMO需求高速增长,细胞治疗CDMO迎来快速发展的机遇。
Lonza Pharma Biotech & Nutrition是全球CDMO龙头企业,以其可靠优质的服务、遍布全球的据点、创新的技术平台和丰富的经验备受认可。CDMO服务涉及临床前阶段到上市的各个环节,包括发现研究、临床前阶段以及临床商业化试验,为艾伯维、BMS、罗氏等大型药企提供CDMO服务。公司2020年实现45亿欧元营收,增长12.2%。细胞治疗CDMO业务的占比逐渐增长,是贡献收入增速最快的板块之一。从Lonza的业务发展趋势可以看出细胞治疗领域是目前全球研发的主流趋势之一,细胞治疗CDMO的收入增长稳定。
全球生命科学服务巨头Thermo Fisher在2019年以17亿美元收购Brammer Bio,进入细胞治疗CDMO服务领域。Thermo Fisher可同时提供细胞治疗CDMO整体解决方案和生物工艺解决方案。实验室产品及服务可提供细胞治疗药物实验室所需产品,同时提供全面的制药和生物技术行业外包服务,用于药物开发、临床试验和商业化生产。其生命科学解决方案提供广泛的试剂、仪器及耗材,覆盖细胞治疗产品的发现和生产全流程。公司2020年实现营收32.2百万美元,Thermo Fisher实验室产品及服务和生命科学解决方案收入占比75.8%,业务收入占比不断提高,2018-2020年生命科学解决方案营收年复合增长率达24.7%。
对于国内市场,谱新生物是中国唯一的专注于细胞治疗CDMO整体解决方案的提供商,以一体两翼的商业模式为客户提供稳定并高效交付的CDMO服务。谱新生物同时具备细胞治疗上游生物工艺解决方案及CDMO服务,包括了上游生物工艺、临床试验及商业化生产,以及发现和生产全流程中使用的试剂、仪器及耗材。
谱新生物,定位于细胞药物CDMO龙头企业,股东包括国家中小企业发展基金、中科院控股国科嘉和基金、海尔资本、华邦健康、中信建投资本等。公司总部位于苏州市吴中区,注册资本1亿元,拥有苏州总部(10000平米GMP厂房)、深圳基地(8000平米GMP厂房在建),初步形成全国布局的生产基地网络布局。美国北卡基地也在建设中,同步进行全球产能布局。
谱新生物聚焦于细胞药物领域,搭建了细胞药物专用质粒构建平台、悬浮无血清病毒生产平台和全封闭的细胞工艺开发平台。拥有多个质粒工艺开发及中试生产的经验,掌握安全可放大悬浮无血清细胞以及一次性反应器慢病毒生产工艺。此外,在免疫细胞CDMO业务领域,谱新生物具有成熟的细胞冻存制剂工艺,灵活的制备工艺路线,配套齐全的封闭设备以及丰富的申报经验。
谱新生物具有独树一帜的创新平台(包括HiLenti™慢病毒平台及HiCellx™细胞技术平台等),是基于MAH制度下第一个细胞治疗药物生产的CDMO厂商产业化转化评估与服务平台。该平台已支持多个合作伙伴成功孵化了多款CAR-T、TCR-T、干细胞等药物。谱新生物2017年推出对外技术服务,拥有150+IIT临床制备经验以及20+医院的合作资源,2021年订单突破1亿元。谱新生物于2021年8月与普米斯生物技术公司就细胞治疗药物委托开发生产达成全面战略合作,凭借其工艺开发能力和细胞药物GMP生产能力,为普米斯的多个新型CAR-T细胞药提供CDMO服务。

(图片源:Frost & Sullivan)
通过打造开发到生产的工艺平台,提供全流程整体解决方案,谱新生物拥有快速实现发现到产品交付的能力。谱新生物提供从包括质粒、慢病毒、细胞工艺生产的CDMO技术服务,服务阶段覆盖从非注册临床(IIT)、新药临床试验申请(IND)、临床到商业化生产的全流程。谱新生物致力于让更多项目更早更快地达到下一里程碑,把更多细胞药物推向市场,造福更多患者,让细胞药物谱写生命新篇章。

苏州市吴中大道1463号越旺智慧谷4号楼