CAR-T 细胞,即嵌合抗原受体 T 细胞,原理是应用患者自身的 T 淋巴细胞,经过实验室重新改造,装载上具有识别肿瘤抗原的受体,体外扩增后再次回输入患者体内,从而识别并攻击自身的肿瘤细胞。 谱新生物专注于细胞治疗药物 CDMO 服务的整体解决方案,搭建了全封闭的细胞工艺开发平台,可以为不同需求的客户提供高品质的细胞 CDMO 服务。
服务内容
CAR-T 细胞 CDMO 服务(HiCellx® 技术平台) | ||||
类别 | 服务内容 | |||
IIT级别 | 1 | 资料支持 | ● 伦理文件 ● 人遗文件 | ● 与IND申报无缝衔接 ● GMP-like车间 ● 记录真实、可追溯 ● GMP-like质量管理体系 ● 200+批次的生产经验 |
2 | 工艺开发 | ● 根据项目要求(可定制) | ||
3 | 工艺确认 | ● 连续3批生产,满足项目设计要求和质量标准 | ||
4 | 保存稳定性 | ● 根据项目要求(可定制) | ||
5 | 运输稳定性 | ● 根据项目要求(可定制) | ||
6 | 细胞生产与检验(GMP-like) | ● 衔接运输 ● 生产规模:200mL~20L(可定制) ● 工艺路线:灵活的工艺设计、可定制 | ||
*注:谱新生物可为客户提供相对灵活的定制化服务,包括但不限于以上服务内容。
服务优势
谱新生物采用 HiCellx® 细胞技术平台,平台优势: • 使用自主研发的细胞冻存制剂 • 配备国际主流封闭自动细胞生产用设备 • 符合注册临床和商业化要求的细胞车间:全 B+A、单向流、Full-GMP • 细胞扩增倍数高,解决了阳性率低和扩增倍数低的问题 • 可灵活适应各种细胞产品的生产和检验 • 具备大量的封闭自动设备的生产经验 • 拥有 200+ 例 IIT 临床样品生产经验 • 已有 NMPA CAR-T 细胞产品的 IND 成功获批经验 • 承接国内注册临床 CAR-T 细胞产品的技术转移和注册临床细胞样品生产经验 |
生产流程
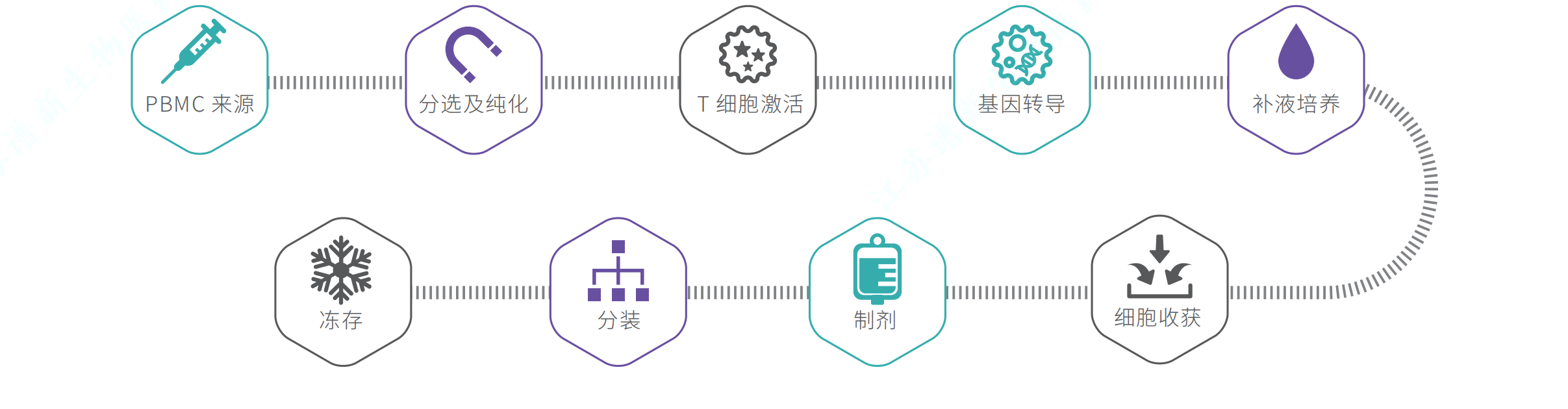
质量控制
类别 | 检测项目 | 检测方法 |
常规检项 | 外观 | 目视法 |
pH | 2020 版ChP 0631 | |
渗透压摩尔浓度 | 2020 版ChP 0632 | |
细胞特性/ 功能检项 | 细胞数量 | 荧光染色 |
细胞活率 | 荧光染色 | |
CAR 阳性率 | 流式细胞术 | |
免疫细胞组成 | 流式细胞术 | |
细胞因子分泌 | 酶联免疫法 | |
细胞杀伤 | 依据方案而定 | |
杂质检项 | 培养过程添加物残留 | 依据添加物类型而定 |
磁珠残留 | 显微观察 | |
安全性检项 | CAR 基因拷贝数 | q-PCR 法 |
细胞内毒素检测 | 2020 版ChP 1143 | |
无菌检测 | 快检 | |
2020 版ChP 1101 | ||
支原体检查 | q-PCR 法 | |
2020 版ChP 3301 | ||
RCL | q-PCR 法 |
*注:谱新生物针对不同技术平台建立了相应的质量控制方法,质量控制检测包括但不限于以上项目。
项目周期
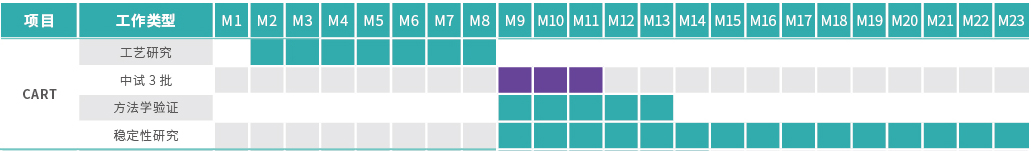
项目管理方案
谱新生物的项目管理团队为每一个GMP 项目保驾护航,团队组成包括项目首席科学家、项目经理、项目QA 和GMP 实施技术专家。

咨询热线:400-900-1882
检测咨询:test@hillgene.com
CDMO服务:bd@hillgene.com
产品咨询:info@hillgene.com
地址:苏州市吴中区吴中大道1463号越旺智慧谷A4号楼整幢

苏州市吴中大道1463号越旺智慧谷4号楼